消化管がんの内視鏡治療により形成される潰瘍を補強する体温応答性コラーゲンが、医学専門誌「消化器内視鏡」にて紹介されました。
弊社は、早期消化管がんに対する内視鏡手術後の偶発症予防を目指し、群馬大学大学院医学系研究科・内科学講座の浦岡俊夫教授らのチームと共同研究を行っています。このプロジェクトでは、術中または術後に形成される潰瘍や穿孔を補強するため、内視鏡を通して使用可能な体温応答性コラーゲンの開発を進めています。
この度、本開発の概要が医学専門誌「消化器内視鏡」(東京医学社)にて紹介されましたのでご報告いたします。このプロジェクトは、日本医療研究開発機構(AMED)の2025年度「橋渡し研究プログラム」・シーズpreFに採択されており、製品化に向けた開発が進行中です。
|
雑誌名 |
消化器内視鏡 (37巻8号) |
|---|
|
著者名 |
群馬大学大学院医学系研究科・内科学講座 浦岡俊夫ら |
|---|
|
題材 |
体温応答性コラーゲンゾルを用いた切除創被覆・補強の試み |
|---|
■ 背景と課題
早期消化管がんの治療においては、ESD(内視鏡的粘膜下層剥離術)などの内視鏡治療が主流であり、日本で開発されたこの方法は、がんの根治と臓器温存を両立し、身体に負担の少ない画期的な治療法として広く普及しています。しかしながらこの治療は、術後に形成される粘膜欠損*1(人工潰瘍)を起点として、後出血*2や遅発性穿孔*3といった重篤な偶発症*4が一定の頻度で生じることが大きな課題となっています。特に、高齢化に伴い出血リスクの高い患者が増加する中、これらの偶発症を確実、簡便、かつ安全に予防できる、費用対効果に優れた新たな医療機器の開発が強く求められています。
*1:早期がん切除後に、病変を剥がした部分の粘膜組織の一部が一時的に傷つき、失われたり剥がれ落ちたりしている状態
*2:内視鏡手術で病変を切除した部分が一時的に潰瘍(傷)となり、この傷口が治癒する過程でおこる出血
*3:内視鏡手術で術後一定の時間が経過してから術部に穴が開く合併症
*4:医療行為を行う際に、予期せず、あるいは不可抗力で発生してしまう、望ましくない病気や症状
■ 開発の目的とアプローチ
本開発は、組織工学(Tissue-Engineering:体の組織を再生・修復する技術)に着想を得ています。術後の潰瘍部に生体吸収性足場(スキャフォールド)*1として機能する体温応答性コラーゲンを、内視鏡を通して導入します。このコラーゲンは、体内でゾル(液状)からゲル(ゼリー状)に変化することで、術後の潰瘍を被覆・補強することが明らかにされました。最終的には組織再生の足場として体内で分解吸収されながら正常な潰瘍治癒を促進します。この革新的な技術を通じて、ESD後の後出血を抑制し、治療の安全性を格段に向上させることを目指します。
*1:体内で溶けて消失する、組織再生のための一時的な土台
■ 体温応答性コラーゲンによる治癒プロセス
1.使用方法
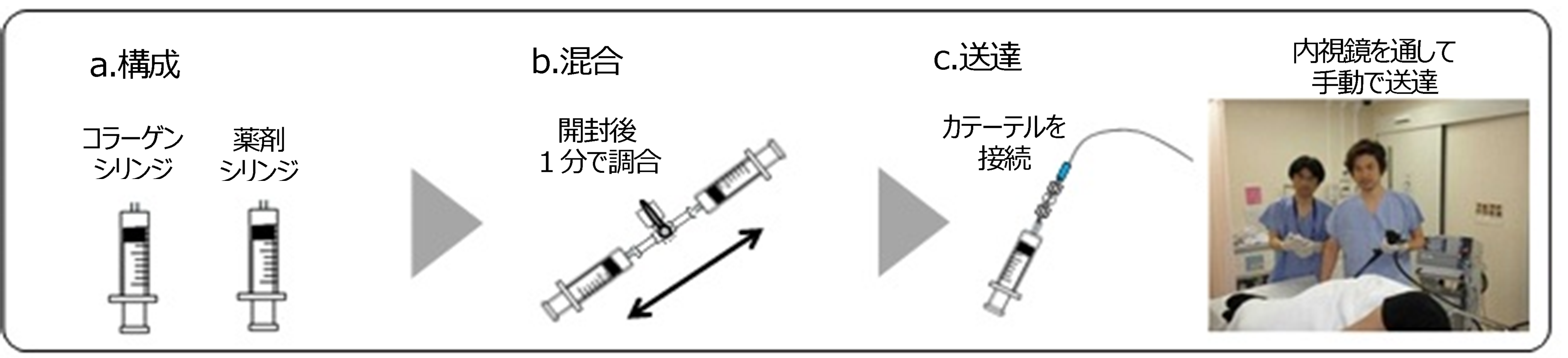
(1)本開発品は、以下の2本のシリンジで構成されています。(図1-a)
・コラーゲン溶液が充填されたシリンジ
・薬剤(架橋剤など)を含むシリンジ
(2)この2本のシリンジをコネクタで接続し、プランジャー(押し子)を交互にプッシュして両液を数回行き来させることで、コラーゲンと薬剤を均一に混合します。(図1-b)
(3)混合が完了したシリンジにカテーテル(細長いプラスチック製チューブ)を接続します。(図1-c)
(4)カテーテルを内視鏡の鉗子口から通路を通して消化管内に挿入し、内視鏡治療によって形成された潰瘍(人工潰瘍、数cmの直径)に向けてコラーゲン混合液を送達(注入・散布)します。
この方法は、コラーゲンの調合と送達が簡易で、特殊な機器や装置を必要としないことが利点です。
図1.体温応答性コラーゲンの使用方法
2.注入後の作用と治癒プロセス
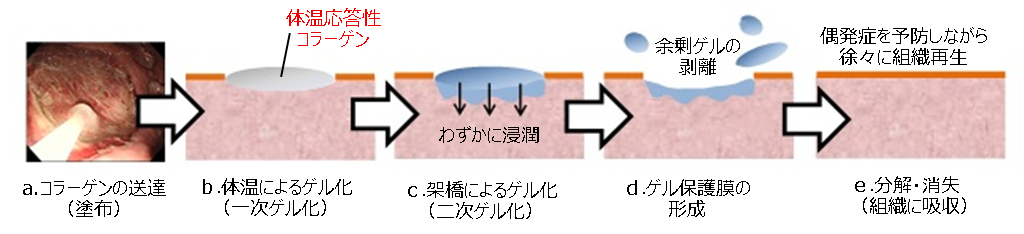
(1)注入されたコラーゲン混合液は、潰瘍表面を速やかに覆います。(図2-a)
(2)体温による温度上昇により、コラーゲンが急速にゲル化(一次ゲル化)します。(図2-b)
(3)その後、コラーゲンは潰瘍部の組織へわずかに浸潤しながら、架橋剤の作用により、さらに強固なゲルを形成(二次ゲル化)します。(図2-c)
(4)過剰なゲルは剥がれ落ちますが、潰瘍表面にはコラーゲンゲルによる保護膜がしっかりと形成されます。この保護膜が潰瘍表面を物理的に補強することで、後出血や遅発性穿孔といった偶発症を防ぐ役割を果たします。(図2-d)
(5)コラーゲンは生体吸収性材料であるため、保護膜としての役割を果たした後、その後の潰瘍の治癒プロセスに取り込まれる形で徐々に分解・消失し、最終的に潰瘍が上皮化(組織再生)することで治癒が完了します。(図2-e)
図2.内視鏡治療による治癒プロセス(イメージ)
■ 実証実験の結果
生体ブタを用いたモデル実験では、体温応答性コラーゲンが、内視鏡治療における以下の二つの重要な機能を果たすことが実証されました。
・ESD術中の穿孔に対する閉鎖材*1として機能すること。
・ESD後の潰瘍に付着し、物理的補強と組織再生の足場材料として機能すること。
*1:体内にできた傷口や穴を塞ぐために使用される医療用の材料や器具。内視鏡治療においては、内視鏡クリップや特殊パッチなどがこれにあたり、体温応答性コラーゲンはこれらの機能を担う
■今後の展望
1.本開発の優位性
開発中の体温応答性コラーゲンは、内視鏡を通して潰瘍を補強する医療材料に求められる理想的な特性と多くの利点を兼ね備えています。室温では流動性を保ち、カテーテルからの送達が可能である一方、体温に反応して急速にゲル化し、潰瘍表面を速やかに覆い保護します。さらに、コラーゲンを固めるための生体安全性に優れた薬剤を使用することで、ゲル保護膜の強度と組織接着性が向上します。また、治療目的に合わせて粘度や硬化速度、ゲル強度の制御が可能である点も大きな特徴です。
2.医療への貢献
この体温応答性コラーゲンは、体内で分解・吸収されるため異物残留のリスクがなく、潰瘍(傷)の治癒過程を妨げません。従来の治療法で必要とされたクリップよりも極めて簡便かつ操作性に優れ、別の内視鏡的治療が必要な場合でも妨げにならないという優れた性質も有しています。現在、実用化に向けてプロトタイプ機の試作を進めており、この革新的なコラーゲンの開発と臨床応用は、安全で簡便な偶発症予防策として、内視鏡切除のさらなる発展に大きく貢献すると期待されます。
■ご参考
この体温応答性コラーゲンは、弊社主席研究員の柚木俊二が浦岡教授とともに長年に渡り実験データを積み上げてきた革新的マテリアルです。これまでに、その安全性および有効性が示唆された複数の論文が国際的な専門誌に掲載されており、本開発の学術的基盤の確かさが裏付けられています。
【主な掲載論文】
Takatori Y, Uraoka T, Yunoki S et al. Potential of temperature-response collagen-genipin sol as a novel submucosal injection agent for endoscopic resection: Acute and chronic phase study using living animals. Digestive Endoscopy. 35: 471–480 (2023)
Uraoka T, Yunoki S et al. Closure of gastric perforations during endoluminal resection using a novel biodegradable collagen sol: A feasibility survival study on porcine model (with video). Digestive Endoscopy. 34: 105–112 (2022)
Uraoka T, Yunoki S et al. Novel temperature-responsive, biodegradable and injectable collagen sol for the endoscopic closure of colonic perforation holes: Animal study (with videos). Digestive Endoscopy. 33: 616–620 (2021)
Takatori Y, Uraoka T, Yunoki S et al. Potential of temperature-response collagen-genipin sols as a novel submucosal injection material for endoscopic resection. Endosc Int Open. 7:E561-E567 (2019)
Narita T, Uraoka T, Yunoki S et al. In situ gelation properties of a collagen-genipin sol with a potential for the treatment of gastrointestinal ulcers. Med Devices (Auckl) 15;9:429-439 (2016)
Yunoki S et al. Temperature-responsive gelation of type I collagen solutions involving fibril formation and genipin crosslinking as a potential injectable hydrogel. Int J Biomater. (2013) Article ID: 620765.

